Notícia
Anvisa habilita primeira empresa importadora de células germinativas e embriões no Brasil
Autorização concedida pela Agência tem como principal objetivo garantir que o material importado tenha qualidade e segurança
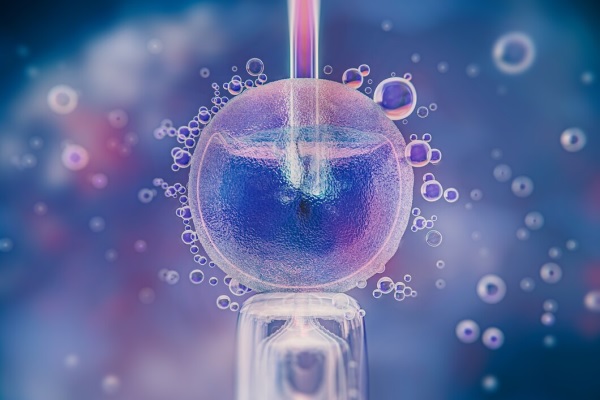
Freepik
Fonte
Anvisa | Agência Nacional de Vigilância Sanitária
Data
quarta-feira, 1 novembro 2023 13:50
Áreas
Bioética. Biologia. Biomedicina. Biotecnologia. Fertilização. Genética. Microbiologia. Vigilância Sanitária.
A Agência Nacional de Vigilância Sanitária (Anvisa) concedeu autorização à Criobrasil Serviços para desempenhar atividades essenciais de importação, transporte e distribuição de células germinativas, tecidos e embriões humanos no território brasileiro. A autorização foi publicada na Resolução RE 4.042/2023.
Este é um passo significativo de um processo iniciado em julho de 2023, no qual a empresa apresentou documentos que demonstraram o cumprimento das disposições da Resolução da Diretoria Colegiada (RDC) 771/2022.
A autorização de empresa importadora está programada para ser renovada a cada dois anos. Também é necessário o envio, a cada seis meses, de relatórios e informações à Anvisa, para garantir a transparência e a aderência contínua aos padrões regulatórios. Além disso, foi concedida à Criobrasil a permissão específica para realizar a importação de amostras seminais do banco estrangeiro Fairfax Cryobank, dos Estados Unidos.
Outros estabelecimentos e Centros de Reprodução Humana Assistida (CRHAs) brasileiros estão engajados no processo de aprimoramento e adequação de seus procedimentos operacionais para serem habilitados.
Reprodução humana assistida no Brasil
Não há uma lei específica no país que discipline a Reprodução Humana Assistida (RHA). A Anvisa recentemente atualizou o marco regulatório que define as Boas Práticas em Células Germinativas, Tecidos Germinativos e Embriões Humanos para uso terapêutico, com a publicação da RDC 771/2022.
O principal objetivo das boas práticas definidas pela Agência é estabelecer requisitos para a segurança e a qualidade das células, tecidos e embriões disponibilizados aos pacientes brasileiros, bem como garantir a segurança dos doadores e trabalhadores desses estabelecimentos.
De acordo com a Resolução, os CRHAs, anteriormente referidos como Bancos de Células e Tecidos Germinativos, devem estar regularizados perante os órgãos locais de vigilância sanitária. Essa regularização é assegurada através de ações contínuas de inspeção sanitária, focadas na verificação rigorosa do cumprimento de requisitos essenciais de segurança e qualidade.
Importação de gametas e embriões pelo Brasil
As técnicas de RHA podem ser realizadas com gametas e embriões doados e processados nos CRHAs brasileiros e por meio da utilização de material biológico proveniente de doadores estrangeiros.
A circulação global de gametas e embriões tem apresentado um aumento significativo nos últimos anos, com grande número de importações destinadas ao Brasil, originárias de diversos países e em grandes volumes.
Por essa razão, tornou-se fundamental estabelecer estratégias e requisitos específicos para garantir que essas células e tecidos sejam importados por empresas especializadas, que assumam a responsabilidade pela atividade de importação, transporte e distribuição desses materiais biológicos, a fim de que eles cheguem com segurança e qualidade para o tratamento dos pacientes brasileiros.
A habilitação das empresas pela Anvisa tem como objetivo primordial avaliar requisitos necessários para garantir que o material importado (sêmen e/ou óvulos) cumpra com especificações de qualidade e segurança mínimas, tais como:
- Seleção adequada das amostras;
- Testagem para doenças infectocontagiosas e doenças genéticas;
- Padronização de técnicas de processamento, avaliação e controle de qualidade;
- Transporte adequado e distribuição das amostras.
Além disso, as empresas importadoras são responsáveis por realizar os controles das gestações, para cumprir com o disposto na Resolução do Conselho Federal de Medicina (CFM), que dispõe que o registro dos nascimentos evitará que um doador tenha produzido mais de dois nascimentos de crianças de sexos diferentes em uma área de 1 milhão de habitantes.
A seguir, destacam-se algumas responsabilidades da empresa importadora habilitada:
- Armazenar, quando aplicável, as amostras importadas antes do fornecimento aosCRHAscontratantes e liberar as amostras importadas;
- A empresa importadora deve avaliar, no mínimo, os seguintes aspectos para cada importação:
-
- Documentação aduaneira;
- Todos os laudos de triagem clínica e laboratorial necessários para avaliar a qualidade e a segurança da amostra importada;
- Regularização atual dos bancos de origem junto às autoridades competentes estrangeiras;
- Regularização dos centros destinatários junto à Vigilância Sanitária (Visa) local; e
- Codificação utilizada em conformidade com os procedimentos padronizados e acordados.
É fundamental avaliar constantemente a adequação dos bancos de origem e seus parceiros terceirizados (laboratórios de análises clínicas, centros descentralizados de coleta, operadores de logística) a fim de garantir a qualidade e a segurança dos materiais importados para o paciente.
Todos os lotes liberados pela empresa importadora às clínicas brasileiras devem ser devidamente revisados quanto aos aspectos relacionados à qualidade, mediante emissão do Certificado de Liberação da Amostra.
Segundo a RDC 771/2022, a importação de células germinativas, tecidos germinativos e embriões humanos ocorre por meio das modalidades de importação do Sistema Integrado de Comércio Exterior (Siscomex), Remessa Expressa ou Declaração Simplificada de Importação. É proibida a importação pelas modalidades de remessa postal, bagagem acompanhada e bagagem desacompanhada.
Acesse a notícia completa na página da Anvisa.
Fonte: Anvisa. Imagem: Freepik.
Em suas publicações, o Canal Farma da Rede T4H tem o único objetivo de divulgação científica, tecnológica ou de informações comerciais para disseminar conhecimento. Nenhuma publicação do Canal Farma tem o objetivo de aconselhamento, diagnóstico, tratamento médico ou de substituição de qualquer profissional da área da saúde. Consulte sempre um profissional de saúde qualificado para a devida orientação, medicação ou tratamento, que seja compatível com suas necessidades específicas.
Os comentários constituem um espaço importante para a livre manifestação dos usuários, desde que cadastrados no Canal Farma e que respeitem os Termos e Condições de Uso. Portanto, cada comentário é de responsabilidade exclusiva do usuário que o assina, não representando a opinião do Canal Farma, que pode retirar, sem prévio aviso, comentários postados que não estejam de acordo com estas regras.





Por favor, faça Login para comentar