Notícia
Sanofi e GSK iniciam testes clínicos de Fase 1/2 de vacina contra a COVID-19 à base de proteína recombinante nos EUA
Estudos pré-clínicos indicam segurança e imunogenicidade promissoras
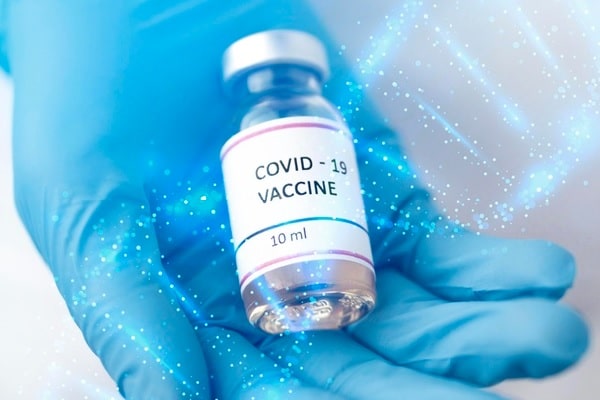
Freepik
Fonte
Sanofi
Data
sábado, 12 setembro 2020 15:55
Áreas
Biotecnologia. Doenças Infecciosas. Estudo Clínico. Farmacologia. Saúde Pública. Vacinas.
A Sanofi e a GSK anunciaram recentemente o início dos ensaios clínicos de Fase 1/2 para a potencial vacina com adjuvante contra a COVID-19. A vacina candidata, desenvolvida em parceria pela Sanofi e GSK, usa a mesma tecnologia baseada em proteína recombinante de uma das vacinas sazonais contra a influenza da Sanofi, combinada com a tecnologia de adjuvante pandêmico estabelecida pela GSK.
A Fase 1/2 dos ensaios clínicos será realizada de maneira randomizada, duplo-cego e controlada por placebo, com o objetivo de avaliar a segurança, a tolerabilidade e imunogenicidade da candidata à vacina. Um total de 440 adultos saudáveis serão envolvidos nos testes, conduzidos em 11 centros de pesquisa nos Estados Unidos.
As empresas estimam que os primeiros resultados da Fase 1/2 do estudo clínico sejam divulgados em dezembro de 2020, possibilitando o início da Fase 3 ainda este ano. Se os dados forem suficientemente promissores, o plano é solicitar a aprovação regulatória da vacina no primeiro semestre de 2021.
A Sanofi está liderando o desenvolvimento clínico e o registro da vacina contra a COVID-19. Dados pré-clínicos mostraram um perfil de reatogenicidade aceitável e dados de duas injeções da vacina com adjuvante recombinante mostraram altos níveis de anticorpos neutralizantes que são comparáveis aos níveis em humanos que se recuperaram da infecção do novo coronavírus. Resultados pré-clínicos serão publicados ainda este ano. Em paralelo, as empresas estão aumentando a produção do antígeno e adjuvante com o objetivo de produzir, após as devidas confirmações e aprovações regulatórias, até um bilhão de doses em 2021.
“A Sanofi e a GSK estão trazendo ciência e tecnologia comprovadas para a luta contra a pandemia global da COVID-19, com o objetivo compartilhado de entregar uma vacina segura e efetiva”, disse o Dr. Thomas Triomphe, Vice-Presidente Executivo e Líder Global da Sanofi Pasteur. “O início do nosso estudo clínico é um passo importante que nos deixa mais próximos de uma vacina em potencial para o combate ao novo coronavírus. Nosso time e parceiros continuam trabalhando incansavelmente, uma vez que queremos entregar os primeiros resultados no início de dezembro. Dados positivos permitirão um início imediato da Fase 3 dos testes até o final deste ano”, destacou o executivo.
“Iniciar os testes cínicos dessa vacina candidata é um progresso importante na busca por conter a pandemia global que estamos vivendo. Essa conquista é baseada na confiança mostrada pelos governos no potencial do imunizante com adjuvante à base de proteína, que utiliza tecnologia estabelecida de ambas as empresas e pode ser produzido em escala por dois dos principais fabricantes de vacinas em todo o mundo. Estamos aguardando os dados do estudo e, se positivos, começaremos a Fase 3 até o final do ano”, afirmou o Dr. Roger Connor, Presidente da GSK Vacinas.
O desenvolvimento da vacina candidata contra a COVID-19 com adjuvante está sendo apoiado por meio de financiamento e colaboração com o Biomedical Advanced Research and Development Authority (BARDA), que é parte do escritório do Secretário Adjunto para Preparação e Resposta do Departamento de Saúde e Serviços Humanos dos Estados Unidos.
Sanofi e GSK estão comprometidas em disponibilizar a vacina globalmente
Em julho de 2020, Sanofi e GSK anunciaram um esforço colaborativo com o governo norte-americano para fornecer até 100 milhões de doses da vacina baseada em proteína recombinante contra a COVID-19, contribuindo para atender a meta da Operação Warp Speed do governo dos Estados Unidos, que visa disponibilizar, o mais rápido possível, centenas de milhões de doses de imunizantes seguros e eficazes contra o novo coronavírus. O governo norte-americano tem a possibilidade de discutir uma nova compra de até 500 milhões de doses a longo prazo. Ambas empresas também acordaram (sujeito a contrato final) com o governo do Reino Unido o fornecimento de até 60 milhões de doses da vacina.
A Sanofi e a GSK planejam fornecer uma parcela significativa do abastecimento mundial para COVAX em 2021/2022, o pilar de vacinas do ACT-Accelerator, uma colaboração global entre governos, organizações globais de saúde, empresas e filantropia para acelerar o desenvolvimento, a produção e o acesso equitativo aos testes, tratamentos e vacinas relacionados ao novo coronavírus.
Acesse a notícia na página da Sanofi.
Fonte: Sanofi Brasil. Imagem: Freepik.
Em suas publicações, o Canal Farma da Rede T4H tem o único objetivo de divulgação científica, tecnológica ou de informações comerciais para disseminar conhecimento. Nenhuma publicação do Canal Farma tem o objetivo de aconselhamento, diagnóstico, tratamento médico ou de substituição de qualquer profissional da área da saúde. Consulte sempre um profissional de saúde qualificado para a devida orientação, medicação ou tratamento, que seja compatível com suas necessidades específicas.
Notícias relacionadas
Os comentários constituem um espaço importante para a livre manifestação dos usuários, desde que cadastrados no Canal Farma e que respeitem os Termos e Condições de Uso. Portanto, cada comentário é de responsabilidade exclusiva do usuário que o assina, não representando a opinião do Canal Farma, que pode retirar, sem prévio aviso, comentários postados que não estejam de acordo com estas regras.





Por favor, faça Login para comentar